Nové Objevy v Biologii: Role Proteinu CENP-E při Dělení Buněk
Vědci objevili překvapující funkci pro klíčový protein zapojený do dělení buněk. Tato zjištění, uvedená v několika publikacích, zpochybňují dlouho přijímané modely a standardní popisy uvedené v biologických učebnicích.
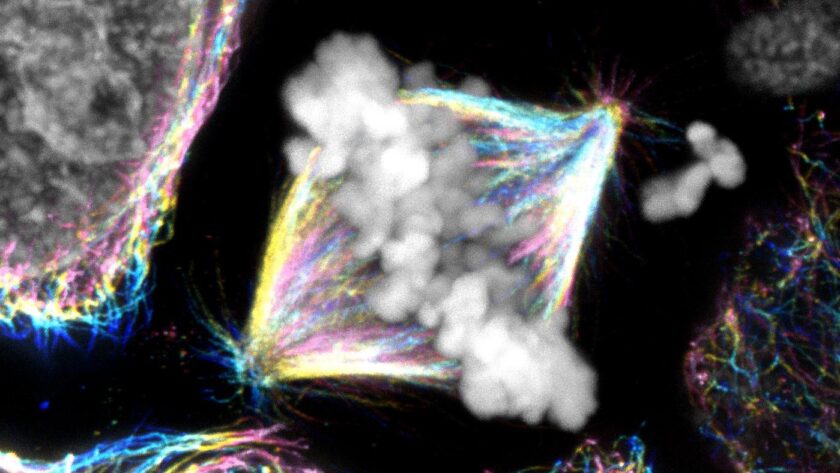
Výzkumníci z Institutu Ruđer Bošković (RBI) v Záhřebu, Chorvatsko, odhalili, že protein CENP-E, dříve považovaný za motor táhnoucí chromozomy do správné polohy během dělení buněk, ve skutečnosti slouží k jinému účelu. CENP-E stabilizuje jejich počáteční spojení s „dráhami“ uvnitř buňky, čímž zajišťuje, že jsou správně zarovnány před tím, než se oddělí.
Ve zmíněné studii vědci také zjistili, že centromery – malé struktury uvnitř buněk, které se dříve předpokládalo, že fungují nezávisle – ve skutečnosti vedou tento esenciální protein, aby pomohly udržet přesné dělení buněk. Toto zjištění převrací více než dvacetileté znalosti učebnic a má významné důsledky pro životní vědy, protože chyby v tomto procesu jsou spojené s rakovinou a genetickými poruchami.
Každou sekundu, triliony krát, vykonává lidské tělo neobyčejný výkon. Jedna buňka se připravuje k dělení, obsahující tři miliardy DNA písmen, a somehow zaručuje, že obě dceřiné buňky zdědí přesné kopie tohoto genetického kódu.
Když tato přesnost selže, výsledek může být katastrofický. I jeden špatně umístěný chromozom může narušit vývoj, vést k neplodnosti nebo spustit rakovinu. Dělení buněk patří mezi nejnáročnější procesy v biologii.
Desítky let výzkumníci věřili, že rozumí alespoň jedné z klíčových součástí zapojených do dělení buněk: CENP-E, popisovaného jako molekulární motor odpovědný za tahání chromozomů do středu buňky, aby zajistil správné dělení. Vysvětlení bylo přehledné, přesvědčivé a nakonec nesprávné.
Nové studie z RBI, vedené Dr. Kruno Vukušićem a profesorkou Ivou Tolić, redefinovaly toto chápání a navrhly nové mechanizmy pro fungování CENP-E. „CENP-E není motor, který táhne chromozomy do centra,“ říká Vukušić. „Je to faktor, který zajišťuje, že se mohou správně připojit na prvním místě. Bez této počáteční stabilizace se systém zastaví.“
Jak to vše funguje? Kdy chromozomy váhají na okrajích? Odpověď spočívá v proteinech Aurora kináz, které působí jako nadměrné semafory. Zasílají buňce signály „červené“, destabilizující raná spojení a brání chromozomům, aby se zamkly příliš brzy na špatném místě.
Tato ochrana zabraňuje chybám blízko pólů buňky, ale také riskuje, že se vyprodukuje příliš mnoho červeného a málo zeleného. Zde vstupuje CENP-E do akce. Tím, že moduluje signály, poskytuje dostatek zeleného světla pro to, aby chromozomy mohly chytit. Jakmile vznikne to první stabilní spojení, zbytek následuje přirozeně: chromozomy se řadí uprostřed, řízeny geometrií vřetena a dynamikou mikrotubulů.
„Nejde o hrubou sílu,“ vysvětluje Tolić. „Jde o vytvoření podmínek pro plynulý chod systému. Klíčová role CENP-E je stabilizovat začátek, a jakmile k tomu dojde, zbytek mitózy se odehrává správně.“
Toto je zásadní posun v rámci chápání: od síly a pohybu k regulaci a načasování. A tento posun má důsledky daleko za učebnicemi.
Pro laiky se tento rozdíl může zdát subtilní. V biologii však detaily hrají klíčovou roli. Chyby v segregaci chromozomů jsou definujícím znakem rakoviny. Tumorové buňky jsou patchworky duplikací a delecí celých chromozomů nebo jejich segmentů, přičemž každá se odvozuje od selhání buněčného dopravního systému.
„Nejde jen o přepisování modelu,“ říká Vukušić. „Jde o identifikaci mechanismu, který přímo souvisí s nemocí. To otevírá dveře pro diagnostiku a přemýšlení o nových terapiích.“
Celý výzkum byl podpořen jednou z nejkonkurenčnějších cen na světě, dotací Evropské výzkumné rady, spolu s podporou Chorvatské vědecké nadace a evropskými rozvojovými fondy.
Objevování skrytých pravidel v chaosu představuje klíčový prvek této studie. Práce týmu z Záhřebu osvětluje jedno z těchto skrytých pravidel. Redefinováním role CENP-E a spojením s jinými procesy uvnitř buněk přináší nové pochopení, jak buňky udržují svůj provoz pod nátlakem.
„Objevením toho, jak tyto mikroskopické regulátory spolupracují,“ říká Tolić, „nejen prohlubujeme naše porozumění biologii, ale také se blížíme ke korekci selhání, která leží na pozadí nemocí.“